中国科大在揭示人类疱疹病毒的基因组包装机制方面取得重大突破
5月30日,《自然》杂志在线发表了中国科大合肥物质科学国家研究中心、生命科学学院刘云涛博士、毕国强教授与合作者的研究论文,该工作利用冷冻电镜首次解析了人类疱疹病毒基因组包装的关键机制以及病毒的DNA基因组结构,有助于预防和控制疱疹病毒引发的多种疾病,并可望改造疱疹病毒用于靶向治疗。
图1.人类I型单纯疱疹病毒(HSV-1)DNA通道蛋白的原子分辨率三维结构(作者:王国燕、马燕兵)
疱疹病毒在自然界中广泛存在,在感染人体后能够引发多种疾病,包括带状疱疹、出生缺陷、多种免疫系统疾病以及癌症。疱疹病毒包括囊膜、中间体蛋白层、衣壳和基因组四层结构,其中衣壳通常被视为一个正二十面体,其上有一个独特的DNA通道,是病毒基因组进出的地方。在疱疹病毒生命周期中,最关键的过程之一就是将DNA剪切酶“召集”到该DNA 通道上,识别、包装和切割双链DNA,最终产生含有基因组的病毒粒子。当病毒基因组在病毒衣壳内装满后,会发出某种信号,从而切除冗余的DNA以完成组装。由于缺乏病毒基因组和衣壳DNA通道的高分辨结构,人们对于病毒粒子的基因组包装过程知之甚少。
利用冷冻电镜解析生物大分子的原子分辨率三维结构已成常态,然而对于疱疹病毒基因组结构以及包装基因组的分子机器(即DNA通道)的结构解析仍旧需要克服诸多困难,例如:1、疱疹病毒颗粒具有巨大的直径,导致对于每个病毒颗粒来说,只有部分区域在冷冻电镜成像时能够很好地处于成像焦平面,极大限制了结构解析的分辨率。2、通常对疱疹病毒结构的解析采用正二十面体对称的重构方式来获得高分辨衣壳结构,但是DNA通道和基因组不符合二十面体对称性。3、DNA具有双螺旋对称,DNA通道蛋白大致具有十二重对称性,而病毒顶点的衣壳蛋白具有五重对称性,这种偶联的对称性不匹配极大地增加了结构解析的复杂度。
为了攻克这一难题,研究人员建立了一套基于连续局部分类和对称性释放的重构方法,有效地从病毒的冷冻电镜照片中重建出DNA通道的原子分辨率结构和大部分基因组的三维结构,发现病毒基因组具有左手超螺旋的缠绕方式和一个无序核心。进而,提出病毒可以通过序列识别和构象传递两种方式感知和传递基因组包装的信号,并发现病毒使用“刚性框架-灵活连接”策略获得不匹配的对称性,这种不对称性导致的棘轮运动可能是病毒DNA转运进出衣壳的结构基础。
理解疱疹病毒DNA转运和基因组包装信号获取和传递的基本规则,一方面有望针对性用于疱疹病毒引起的疾病的预防和控制;另一方面,这些发现有助于对疱疹病毒进行改造,使其成为更实用的载体工具,并用于靶向治疗或大脑神经环路示踪等。此外,病毒这种通过DNA超螺旋组装方式来减轻基因组组装过程中的DNA变形扭矩,对于揭示细胞的基因组组织结构有借鉴意义。
该研究展示了疱症病毒完整的非对称结构,获得了第一个真核生物病毒的DNA通道原子模型,也是第一次探测到DNA在通道里的扭曲状态。审稿人评论说,“作者采用最前沿的局部分类方法对疱疹病毒结构的完美解析,堪称高分辨冷冻电镜三维重建的匠心力作。”
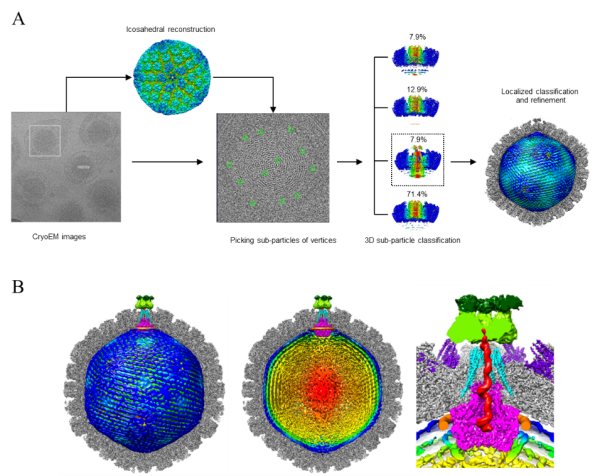
图2.基于连续局部分类和对称性释放的高分辨冷冻电镜三维重构方法(上图);完整人类单纯疱疹病毒(HSV-1)的DNA通道蛋白和DNA基因组高分辨三维结构(下图)
这是中国科大合肥国家研究中心集成影像中心的又一里程碑式研究成果。集成影像中心是合肥物质科学国家研究中心与生命科学学院为推进交叉学科发展而建设的创新研究与公共技术平台,由毕国强教授与中国科大81级校友周正洪博士共同负责筹建与运行管理,初期由两位教授联合培养的博士生张小康(现为浙江大学冷冻电镜中心副教授)具体负责规划和建设,中心于2009年开始建设,2010年底正式投入运行。
经过近十年的发展,集成影像中心率先在国内建立了完善的多尺度、多模态显微成像的技术方法与平台,并培养了多位掌握前沿交叉学科技术的青年科学家。近年来,特别是近两年来已发表十余篇高水平研究论文,在高分辨冷冻电镜、冷冻电镜断层重构原位成像、光电关联显微成像、光学超分辨活细胞成像、跨尺度荧光显微三维重构成像等前沿技术的发展达到了国际领先或一流水平,并在应用前沿显微成像技术解析生物大分子高分辨结构、神经突触超微结构与全脑功能图谱等方面取得了一系列重要突破。集成影像中心经过多年的发展与探索,成为集前沿显微成像技术发展与应用、人才培养和公共技术支撑为一体的创新研究与前沿技术平台。
该研究得到科技部、物质科学国家研究中心的支持。集成影像中心、生命学院星云生物信息平台为此项目提供来计算支持。
论文链接:https://www.nature.com/articles/s41586-019-1248-6
(合肥物质科学国家研究中心、生命科学学院、科研部、新闻中心)


